گزارش رسمی بررسی واکسن کرونا فایزر توسط سازمان غذا و داروی آمریکا (FDA)، اخبار خوشحال کننده و هیجانانگیزی را به همراه دارد؛ در بررسی این موضوع با ما همراه باشید.
خبر رسیده که سازمان غذا و داروی آمریکا (FDA) کار بررسی واکسن کرونا فایزر را پیش برده و گزارش رسمی و جدید منتشر شده در این رابطه، اخبار خوشحال کنندهای را برای مردم جهان به همراه دارد.
گزارش بررسی واکسن کرونا فایزر
فایزر (Pfizer) یک کمپانی داروسازی آمریکایی بوده که با همکاری شرکت دیگری به نام بیونتک (BioNTech)، از همان ماههای اولیه شروع همهگیری کووید 19، واکسنی برای مقابله با این بیماری مرگبار دستگاه تنفسی ساخت. همانطور که انتظار میرود، موفقیت ابتدایی مورد نظر در ساخت دارو به این معنا نبود که میتوان به سرعت واکسن را به عموم مردم تزریق کرد و از آن زمان تا چند هفته پیش، این دو کمپانی داروسازی مشغول آزمایش محصول خود روی گروههای مختلفی از داوطلبان بودهاند.
در واقع کسب اطمینان از ایمنی و کارایی یک واکسن جدید در شرایط آزمایشگاهی، در سه فاز مجزا انجام میشود که فاز سوم آن، چند ده هزار داوطلب را در معرض داروی ساخته شده قرار داده و عملکرد دارو را در سطحی گسترده و روی اقشار مختلف جامعه امتحان میکند. انجام همین فاز برای واکسن کووید 19 فایزر چند هفته پیش به صورت رسمی به پایان رسید و نتایج خوشحال کننده آن در گزارشهای ابتدایی و نهایی به مخاطبان ارائه شد.
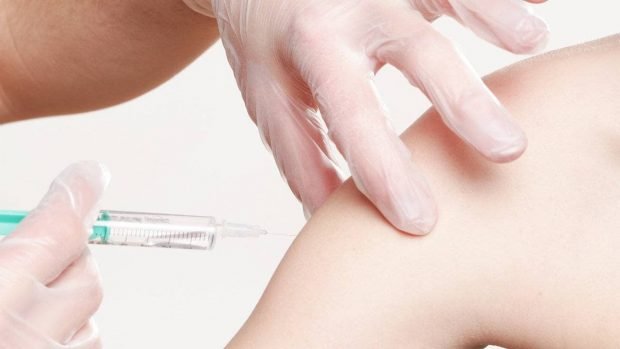
دانشمندان با بررسی واکسن کرونا فایزر گفتهاند که در فاز سوم آزمایش، تست دارو روی بیش از 20 هزار نفر ثابت کرده که این واکسن در 95 درصد مواقع جلوی ابتلای افراد به کووید 19 را میگیرد. کمی پس از انتشار این خبر، فایزر و بیونتک اعلام کردند که در اواخر نوامبر همین سال واکسن خود را برای کسب تاییدیه سازمان غذا و داروی آمریکا ثبت کرده و تا صادر شدن اجازه اضطراری استفاده از دارو توسط این سازمان، صبر خواهند کرد.
صدور اجازه اضطراری
این اجازه اضطراری با نام “EUA” هم شناخته میشود و از زمان شروع همهگیری، FDA در شرایطی ویژه چنین تاییدیهای را برای داروها، فرآیندهای درمانی و تجهیزات مختلف پزشکی صادر کرد. در واقع تاییدیه EUA برخلاف تاییدیههای معمولی این سازمان که مدت زمان نسبتا طولانی برای کسب آنها سپری میشود، در فاصلهای کوتاه پس از ثبت درخواست و با توجه به شرایط اضطراری موجود، صادر میشود.
البته چنین مسئلهای به این معنا نیست که سازمان غذا و دارو بدون رعایت اصولیترین فاکتورها برای تایید یک داروی جدید برای یک بیماری ناشناخته، اجازه رسمی مورد نظر را به فایزر و بیونتک میدهد و عملا حتی با وجود کارایی 95 درصدی واکسن مورد نظر و گزارش نشدن هیچ گونه آثار جانبی خطرناکی در داوطلبان، سختگیریهای خاصی در این رابطه وجود دارند.
با این تفاسیر به نظر میرسد که بررسی واکسن کرونا فایزر توسط کارشناسان FDA نتایج خوشحال کنندهای که در انتظار آنها بودیم را به همراه داشته و تیم دانشمندان این سازمان با بررسی دقیق دادههای جمعآوری شده توسط این دو کمپانی داروسازی، گزارش رسمی خود را در روز سه شنبه گذشته منتشر کردهاند.
طبق اطلاعات موجود، واکسن کووید 19 فایزر که با نام رسمی “BNT162b2” شناخته میشود، از نوع واکسنهای آر ان ای پیامرسان (mRNA) بوده و باید در دو دوز مجزا و با فاصله دو هفتهای، به افراد تزریق شود. کارشناسان میگویند که فرآیند ابتلای افراد به کووید 19 در مدت زمان دو هفتهای پس از تزریق اولیه متوقف میشود و تا مدت زمان 2 ماه پس از تزریق دوم، همچنان دیده شده که افراد در مقابل ویروس کرونا مصون هستند.
عملکرد واکسن کووید 19 ساخته شده
از طرف دیگر تفاوت خاصی در عملکرد واکسن بین جنسیتها، نژادها و سنین مختلف دیده نشده و در میان آثار جانبی که چند هزار داوطلب مصرف داروها گزارش کردند، دردهای خفیف و تب جزو اصلیترین موارد بودهاند. حداقل سن افرادی که در آزمایش واکسن کووید 19 فایزر شرکت کرده بودند، 16 بود و گفته شده که حدودا نیمی از داوطلبان 16 تا 55 سال دچار سردرد، دردهای دیگر و یا تب شدهاند. با این وجود هیچ آثار جانبی خطرناک، عجیب و کشندهای در میان داوطلبانی که از واکسن BNT162b2 استفاده کرده بودند، مشاهده نشد.
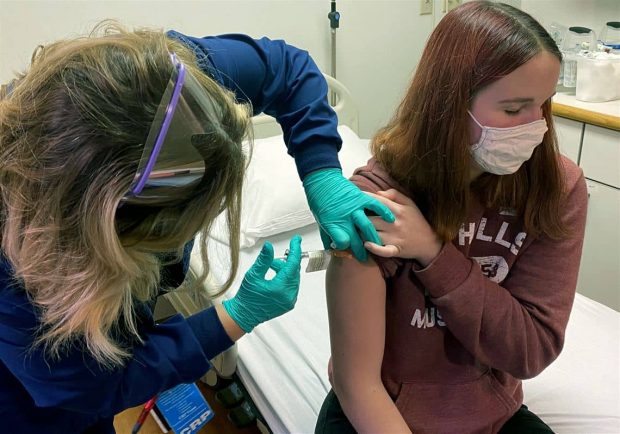
البته گزارش بررسی واکسن کرونا فایزر به ما میگوید که دادههای تهیه شده توسط کمپانیهای مورد نظر محدودیتهایی هم دارند؛ بزرگترین محدودیت اشاره شده، مصونیت دو ماههای بوده که با تزریق دارو ایجاد میشود و کارایی واکسن فراتر از دو ماهی که داوطلبان تحت نظر دانشمندان فایزر و بیونتک بودند، مورد توجه قرار نگرفته است.
چنین موضوعی بیش از همه به خاطر سرعت عمل مورد نیاز برای توسعه واکسن بوده و نمیتوان انتظار داشت که تنها در کمتر از 10 ماه پس از اعلام پاندمی بودن همهگیری اخیر، دارویی ساخته شود که از همه لحاظ کارایی شگفتانگیزی داشته و هیچ نقطه ضعف یا محدودیتی نداشته باشد. از طرف دیگر، حتی اگر FDA تاییدیه اضطراری مورد نظر را برای واکسن کووید 19 فایزر صادر کند، تحقیقات دانشمندان برای مشخص کردن جزئیات تاثیرات بلند مدت استفاده از این دارو همچنان ادامه خواهد داشت و پژوهشهای مورد نظر به همین جا محدود نخواهد شد.
توصیههای مهم با بررسی واکسن کرونا فایزر
یکی دیگر از مهمترین نکاتی که در این رابطه مطرح میشود، وضعیت کسانی بوده که از واکسن BNT162b2 استفاده میکنند؛ به بیان دیگر مشخص نیست که افراد مبتلا شده و نجات یافته از کووید 19 هم باید چنین داروهایی را مصرف کنند و یا آلودگی قبلی آنها مصونیتی را به وجود آورده که دیگر نیاز آنها به واکسن را از بین میبرد.
بررسی واکسن کرونا فایزر توسط سازمان غذا و داروی آمریکا نشان داده که نجات یافتگان کووید 19 هم میتوانند از مزایای تزریق واکسن استفاده کنند. کارشناسان FDA میگویند که یک بار مبتلا شدن به این بیماری مرگبار دستگاه تنفسی به معنی مصون شدن در مابقی عمر نبوده و افراد مورد نظر بعدها هم در معرض آلودگی قرار خواهند گرفت.
گفته شده که سازمان غذا و دارو تصمیم گرفت که در پنج شنبه این هفته جلسهای علنی را برای بررسی واکسن کرونا فایزر برگزار کند؛ FDA پس از این جلسه رسما تصمیم خواهد گرفت که اجازه اضطراری مورد نیاز برای استفاده عمومی از واکسن فایزر را صادر کند یا خیر.
فایزر و بیونتک اعلام کردهاند که تا پایان 2020 مقدار 50 میلیون دوز را که برای واکسینه کردن 25 میلیون نفر کافی بوده، حاضر خواهند کرد و این میزان برای استفاده در سطح جهانی آماده خواهد بود. برای سال 2021 هم این دو کمپانی داروسازی میزان 1.3 میلیارد دوز را برای استفاده مردم جهان آماده میکنند.
 گجت نیوز آخرین اخبار تکنولوژی، علم و خودرو
گجت نیوز آخرین اخبار تکنولوژی، علم و خودرو 

مگه آمریکا فقط
درود بر امریکای بزرگ
دست مریزاد زنده باد آمریکا خبر خوشحال کننده ای بود مرسی گجت نیوز☘☘☘☘